
|
|
|
超音波診断装置用 ロボットシステム WTA-2R |
|
|
Waseda Tokyo Women's Medical Aloka
Blood Flow Measurement Robot System No.2 Refined |
|
|
1.研究背景
2.ハードウェア構成 3.プローブ自動位置決めアルゴリズム 4.評価試験 5.謝辞・リンク |
腹部超音波診断アシストロボット
研究業績 高西研ホーム |
1.研究背景
日本人の死因
|
日本人の約6割が三大生活習慣病である悪性新生物(ガン),心疾患(心臓病),脳血管疾患(脳卒中)で
亡くなっている.(右図参照) |
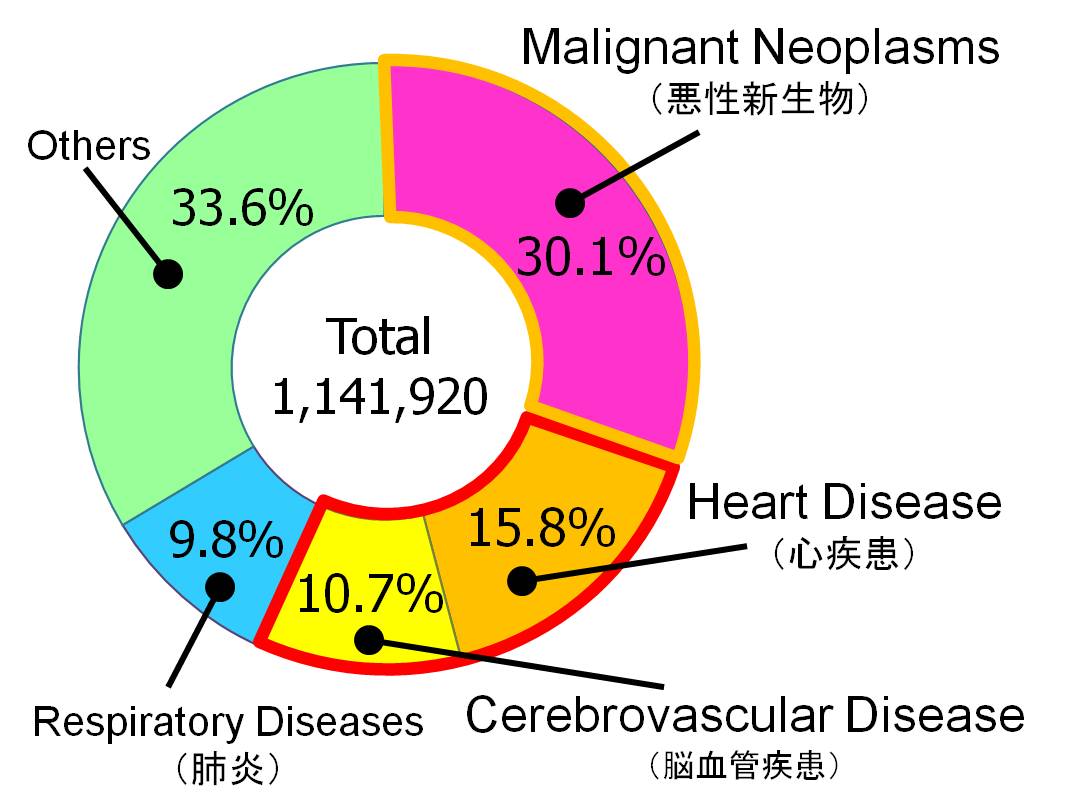
2009年度人口動態統計(厚生労働省)
|
Wave Intensity
|
Wave Intensityは心臓から抹消へ向かう前進波と抹消から心臓へ向かう反射波による合成波形である動脈の血圧と
血流速度の波形がどちらの影響が優勢であるカを判別する指標としてPakerとJonesが提案した指標であり,
音波の強度と同じ単位であることからそのように呼ばれるようになったものである.
WIはその正負の符号が持つ物理的意味(前進波と反射波の影響の優劣)にのみ注目されてたが,
姫路獨協大学の菅原教授の研究によりWIの大きさが重要な生理学的意味を持つことが明らかになり,
血流力学の新たな指針として注目されている. 動脈硬化の進行度合は右図のCompression Wave(以下,W1)とExpansion Wave(以下,W2)の大きさに影響を与える. 動脈硬化が進行し血管が硬くなるにつれてW1の大きさは減少し,W2の大きさは増加する. W1とW2は次式のように表される. 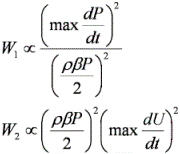
|
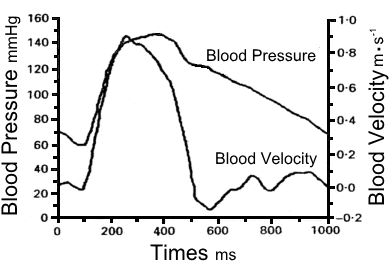
血圧・血流速図
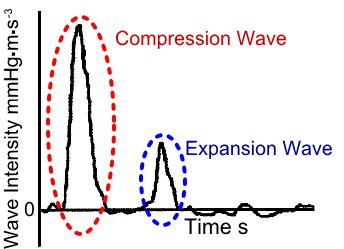
Wave Intensity図
|
WI計測の問題点と本研究の目的
従来のWIの計測方法としては,超音波プローブを手で支える方法や,固定器具で支える方法がとられてきた.
手で支えた場合では,位置調整は容易であるが,WI計測では頸動脈の非常に狭いスポットに一定時間保持し続ける必要があり,
わずかなずれでも計測がやりなおしとなるため,医師・技師の負担が大きく,また,再現性に問題があった.
一方,固定器具を用いた場合は,位置保持の負担は小さいが,微調整が困難で操作性が悪く,計測点がずれるたびに
調整しなおさなくてはならず,かえって計測時間の長大化を招いて患者の負担を増加させているという問題があった.
そこで,本研究ではWI計測にロボットシステムを導入することで,
しっかりとした固定と操作性のよい微調整をマスタスレーブ方式により実現し,計測時間の短縮と医師・患者の負担の軽減を達成するとともに,
画像情報を用いたプローブ自動位置決めアルゴリズムを実装した.
クリックで再生
フリーハンドでのWI計測 |
クリックで再生
固定具を用いたWI計測 |
2.ハードウェア構成
WTA-2R概要
超音波診断装置用ロボットシステム(WTA-2R)は,プローブ保持ロボット,
コントローラ,超音波診断装置,制御PCから成り立っており,その全体図は下記のようになっている.
プローブ保持ロボットは,
頸部血流計測用パラレルリンクマニピュレータ部(以下:マニピュレータ)が取り外し可能となっており,
WTA-2の押し込み補助や
腕吊補助に交換することが可能である.
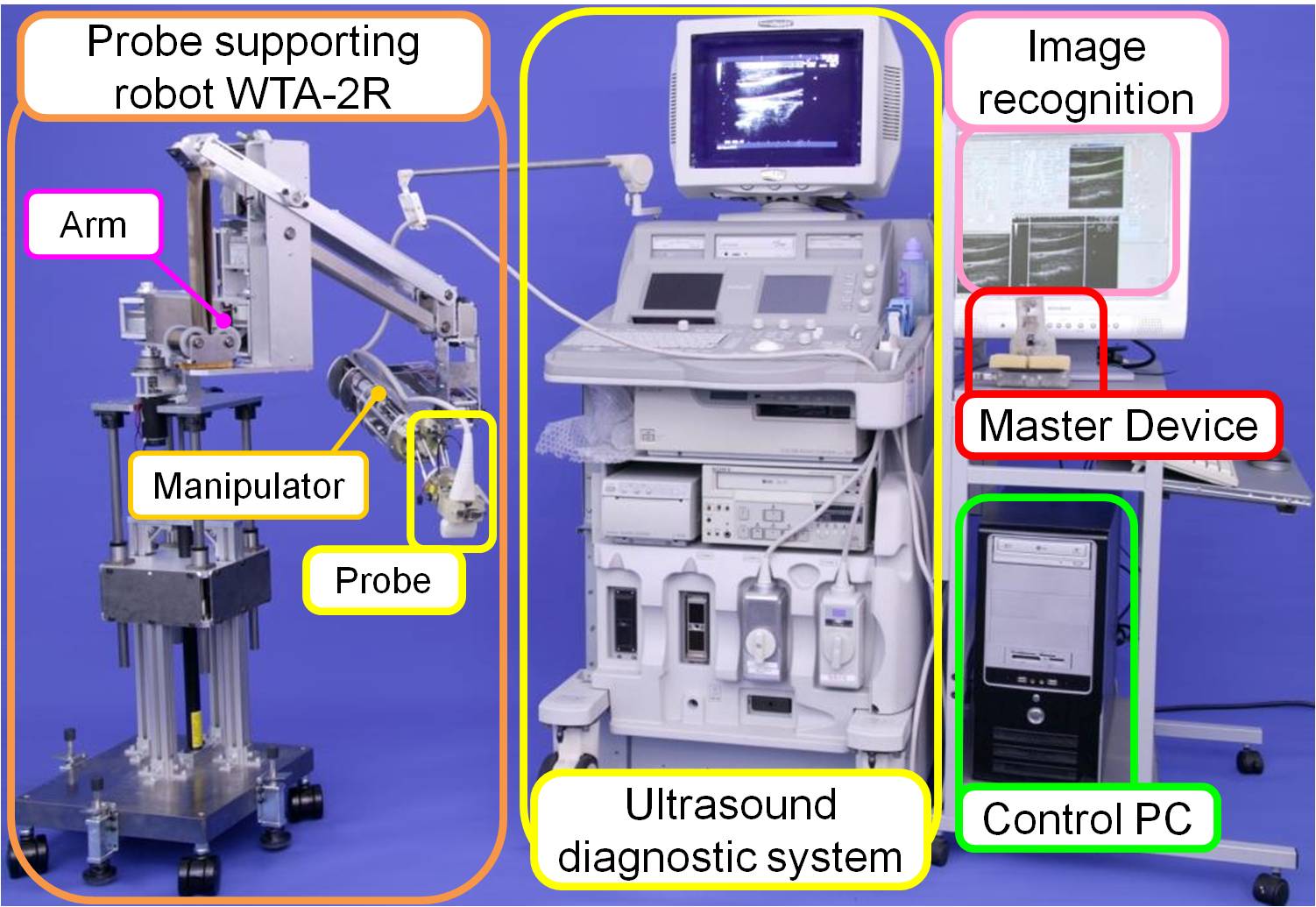
(1)プローブ保持ロボット

プローブ保持ロボット
|
大まかな位置合わせ 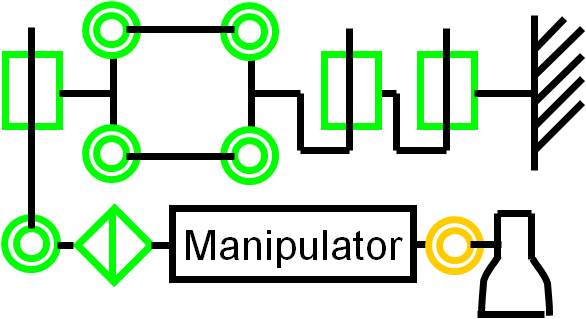
自由度配置図
|
ⅰ) マニピュレータ
|
マニピュレータは,直動型6自由度パラレルリンク機構を有しており,先端にプローブホルダが付属している.
パラレルリンク機構のリンク部はスチュワートプラットフォーム型と似ているが,
違う点はリンク部とアクチュエータ部に分かれていることである.
このような構成にすることにより,リンクを細くすることが可能となり,リンク同士が干渉しにくくなるので,
可動範囲を広く取れるようできる. |
|

マニピュレータ
アクチュエータ
リニアアクチュエータはDCモータとボールねじから構成されており,
ボールねじの送りにより,ボールスプラインを伸縮させている. |
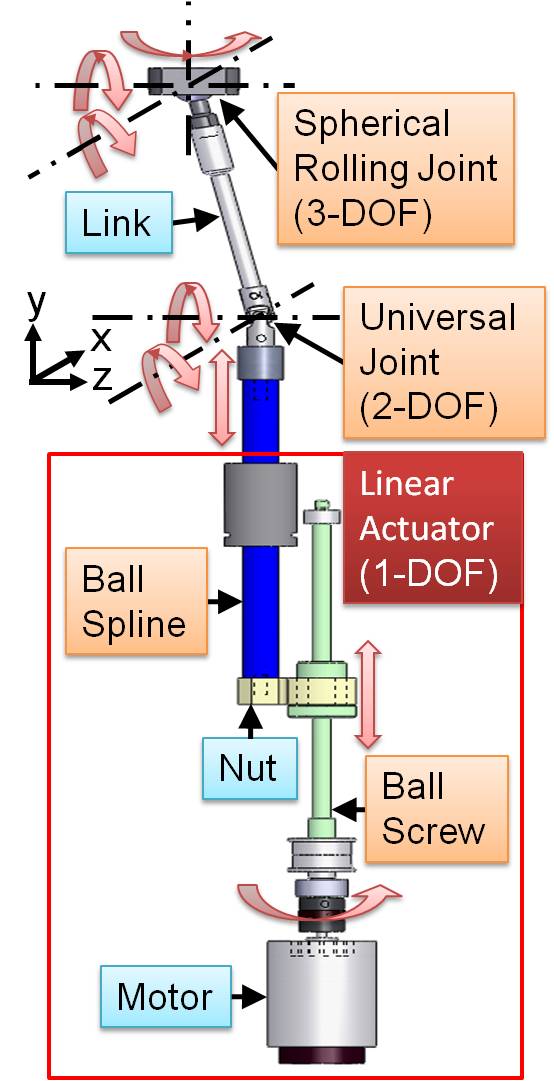
アクチュエータ
|
ⅱ) プローブホルダ
|
プローブを保持することと,マニピュレータとの間に1自由度のジョイント
を設けることを目的とした機構である.ギアと板ばねから構成されており,
2つががかみ合うことで固定することができる.
固定角度は,ギアの歯間の角度10[deg]きざみ,
プローブの姿勢をx軸回りに±45[deg]の間で変化させることができる. |

プローブホルダ
|
ⅲ) アーム
アームは動力を持たないパッシブなシリアルリンク機構で全6自由度を有しており,
各関節に備わる無励磁作動電磁ブレーキで任意の姿勢で固定することが可能である.
アームの自重は根元の定荷重ばねで補償しており,鉛直方向の移動も軽く動かすことが可能である.
無励磁作動電磁ブレーキは,スイッチを押している間だけ固定が解除されるため,
スイッチを切り忘れて固定が解除されたままになる危険性や,
停電などの非通電時にアームがフリーになったままになるという事故が起きない.
また,ブレーキの固定力は人の力で動かせる程度であるため,
医師や患者が危険を感じた場合に固定状態でもすぐにアームを移動させることができる.
自重補償機構は,関節左右のモーメントアームをつりあわせるためスライドガイド上に定荷重ばねを配置することにより構成した.
また,ばね荷重の非直線性を補償するため,スライドガイドの傾きを微調整できるようにした.
これにより,ほぼ完全な自重補償となっている.

アーム
|
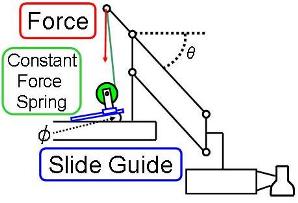
自重補償
|
(2)コントローラ
プローブコントローラにはレーザーマウス,加速度センサ,ジャイロセンサ,フォトセンサを用いている.
X,Y軸方向の並進にはレーザーマウスを用い,Yaw軸回転は2つのレーザーマウスを組み合わせることで検出する.
Roll,Pitch軸回転は加速度センサとジャイロセンサを用いている.Z軸方向並進はフォトセンサで検出する.
コントローラを把持部と接地部に分けることで角度入力をしたときにレーザーマウスが地面から離れてしまう事を防いだ.
また,マイクロコントローラ(以下:マイコン)を用いてPCとUSBにてデータ通信できるようになっている.
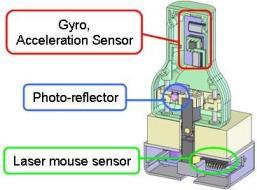

コントローラ
|

クリックで再生
マスタスレーブ動作 |
(3)モータドライバ
マニピュレータを動かすのに,マイコンを用いた小型で電流制御可能なモータドライバを開発した.
このモータドライバにより,配線は,USB,電源,モータ・エンコーダにつなぐケーブルのみになった.
また,6個のモータを同時にUSBを用いて制御することが可能なため,ノートPCでも操作することが可能である.

モータドライバ
|
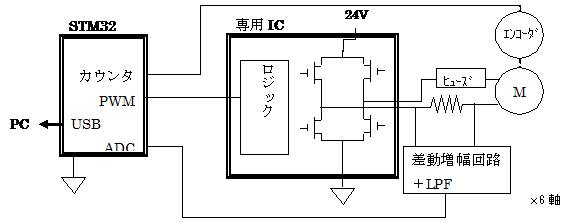
モータドライバ回路構成
|
3.プローブ自動位置決めアルゴリズム
本ロボットシステムはマスタスレーブ方式でプローブの位置決めが可能であるが,さらなる技師負担の軽減のため, 超音波画像情報を用いた頸動脈上へのプローブ自動位置決めアルゴリズムを開発した. WI計測に必要なロボットの頸動脈自動探索アルゴリズムの仕様としては, 可動範囲内に頸動脈が入る位置にロボットをセットすると,ロボットが自動的に WI計測に必要な画像(下記①~④)を探索,描出し, さらに計測中に,画像がそれらの条件(下記①~④)を満たさない状態になった場合, 速やかに回復するシステムである.
WI計測に必要な画像
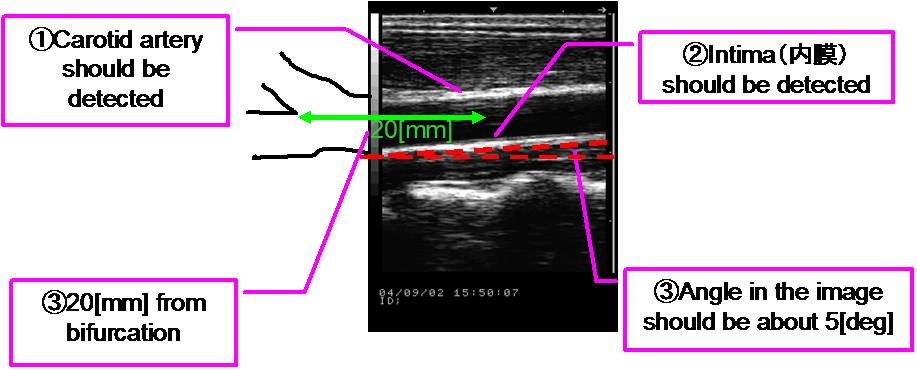
WI計測に必要な超音波診断画像
|
WI計測に必要な画像の要件は以下の4点である. |
頸動脈検出
頸動脈長軸断面は,超音波断層画像中では白いほぼ平行の2線に挟まれる黒い領域が
左右を横断する画像として描出される.血管壁は輝度の高い(白い)領域として描出され,
血液の流れる内腔は輝度の低い(黒い)領域として描出される.多くはほぼ直線状であるが,
多少の湾曲を伴う場合もある.血管は表皮から突出することはありえず,
極端に蛇行することも稀であるので,ほぼ確実に画像の左右端を横断する.
よって,画面を縦方向に走査すれば必ず頸動脈に突き当たるはずである.
また,輝度の高い(白い)線は頸動脈壁以外にも出現しうるが,
黒い帯状の領域が画面の左右を往復するのは頸動脈・頸静脈および皮下組織の3つ以外にはほぼない.
これらを踏まえてアルゴリズムを設計した.
(b).jpg)
頸動脈検出画像処理
(左:(a),右:(b)) |
アルゴリズム(概要)
①一定間隔の縦線上を上から下までスキャンし輝度に閾値を適用して低輝度域を抽出する(右図(a)). |
内膜検出
|
内膜の検出は,血管中心を超音波ビームが捕えているかどうかの判定基準とされている.
動脈壁は外側から外膜,中膜,内膜の3層構造をなしており,超音波断層画像中では一般に外膜,
内膜が高輝度(白色),中膜が低輝度(黒色)で描出される.
しかし,超音波ビームが血管壁に垂直に当たっていないと描出が不鮮明になり,
一般に外膜しか描出されない. |
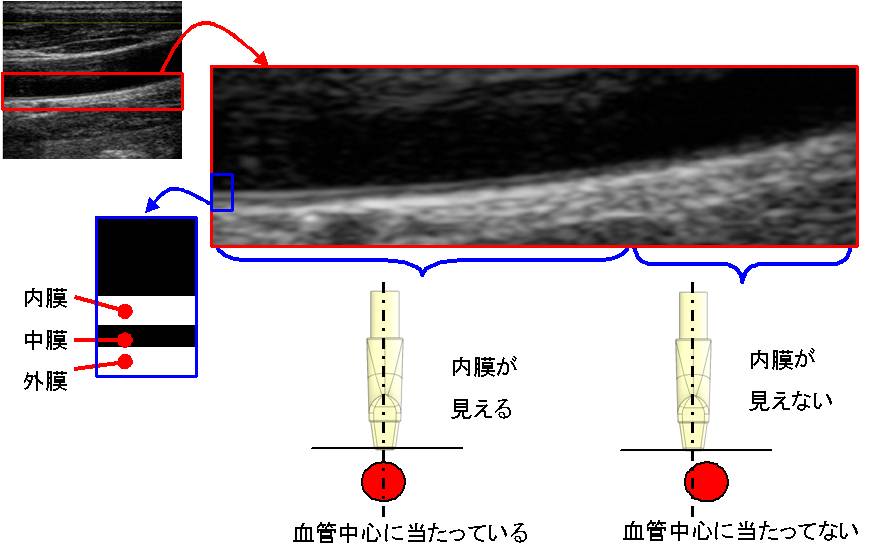
内膜検出の意義
|
プローブ動作
|
プローブの動作を下記のように作成した. スキャン中,頸静脈を誤検出してしまうことがあるため,内圧の差を利用して判断する. プローブで皮膚表皮を圧迫し,その前後の頸動脈径変化を計測し,径が小さくなっていれば静脈と判断(下右図:頸静脈判定). |
||
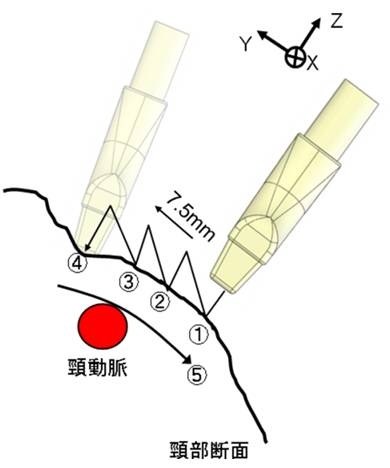
皮膚座標取得と頸動脈探索
|
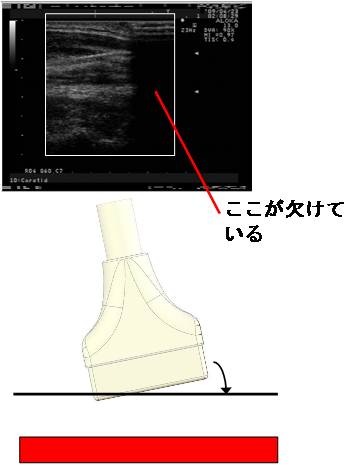
プローブ姿勢修正
|
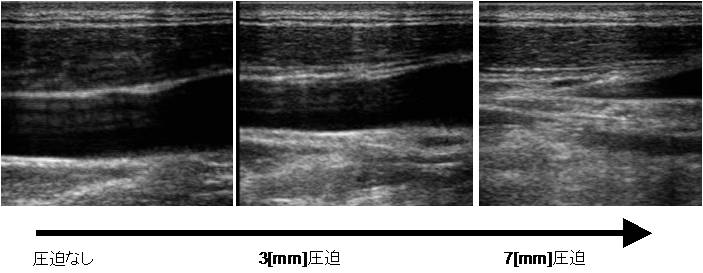
頸静脈判定
|
|
⑤分岐点位置設定 |
||
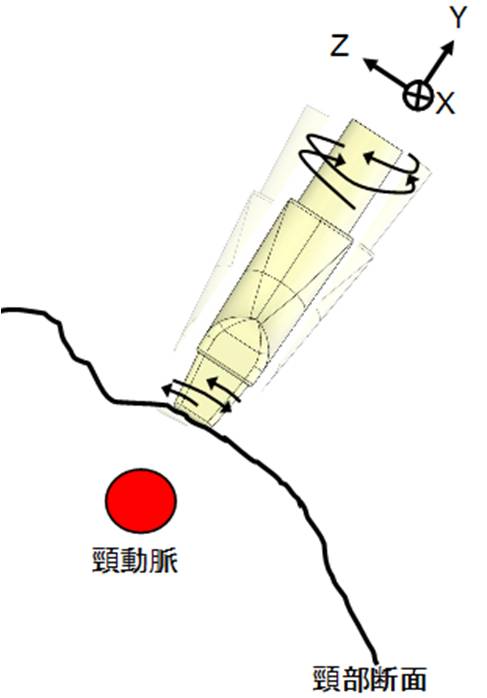
角度調整
|
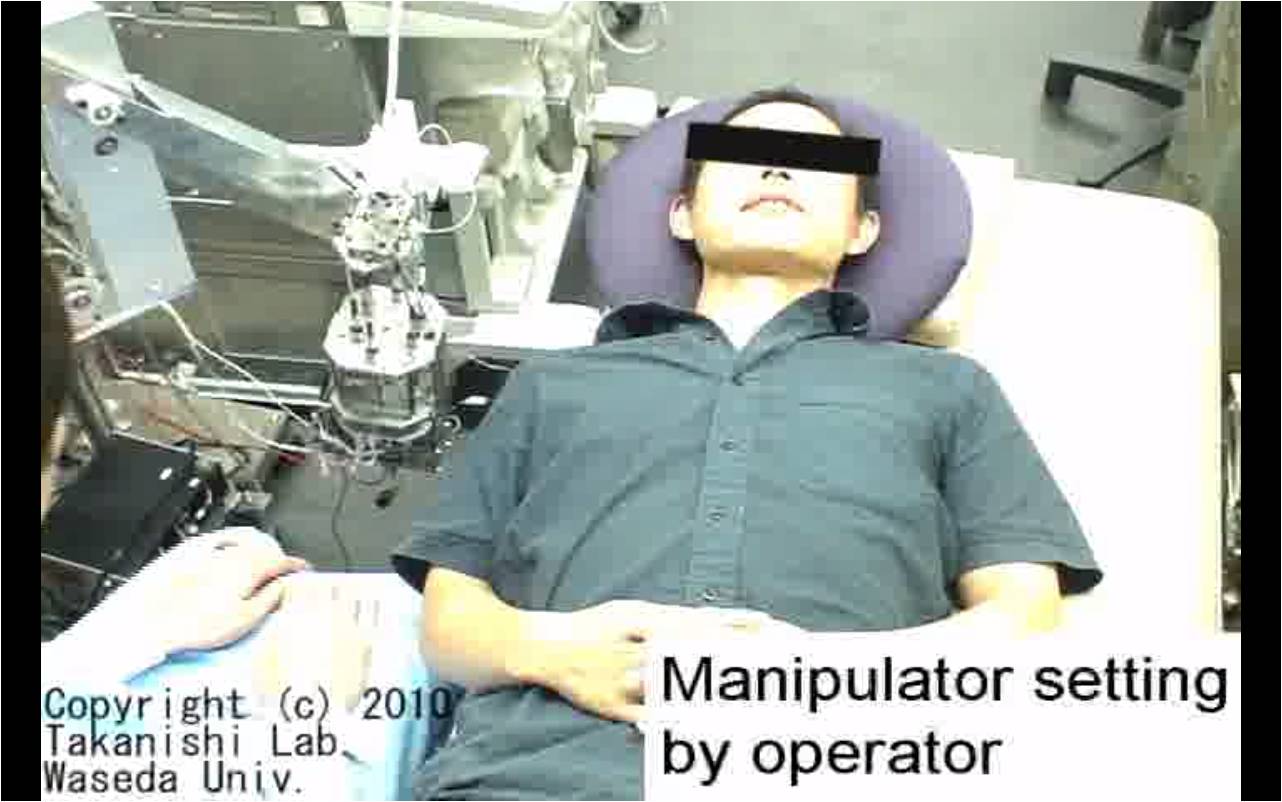
クリックで再生
プローブ自動位置決め動作 |
|
4.評価試験
(1)位置決め精度測定
|
マニピュレータの位置決め精度を光学3次元測定装置(Optotrak)を用いて測定した. |
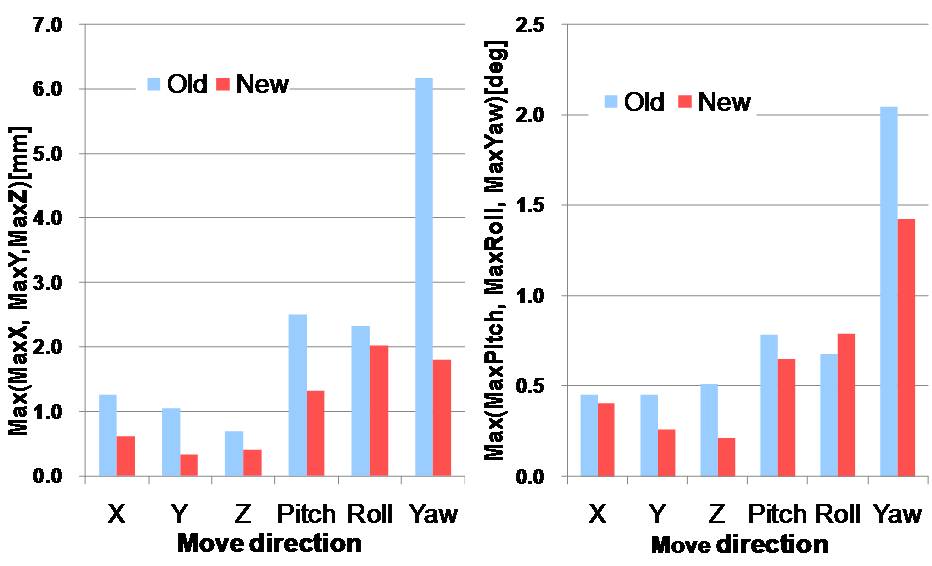
絶対位置精度誤差結果
|
(2)操作性試験(マスタスレーブモード)
|
操作性評価試験として,超音波診断技師5名に,本ロボット(WTA-2R)と旧型機(WTA-2)を用いて
頸動脈の検出を行っていただき,それに要する時間の測定と,操作性等についてのアンケートによる評価を行った. |
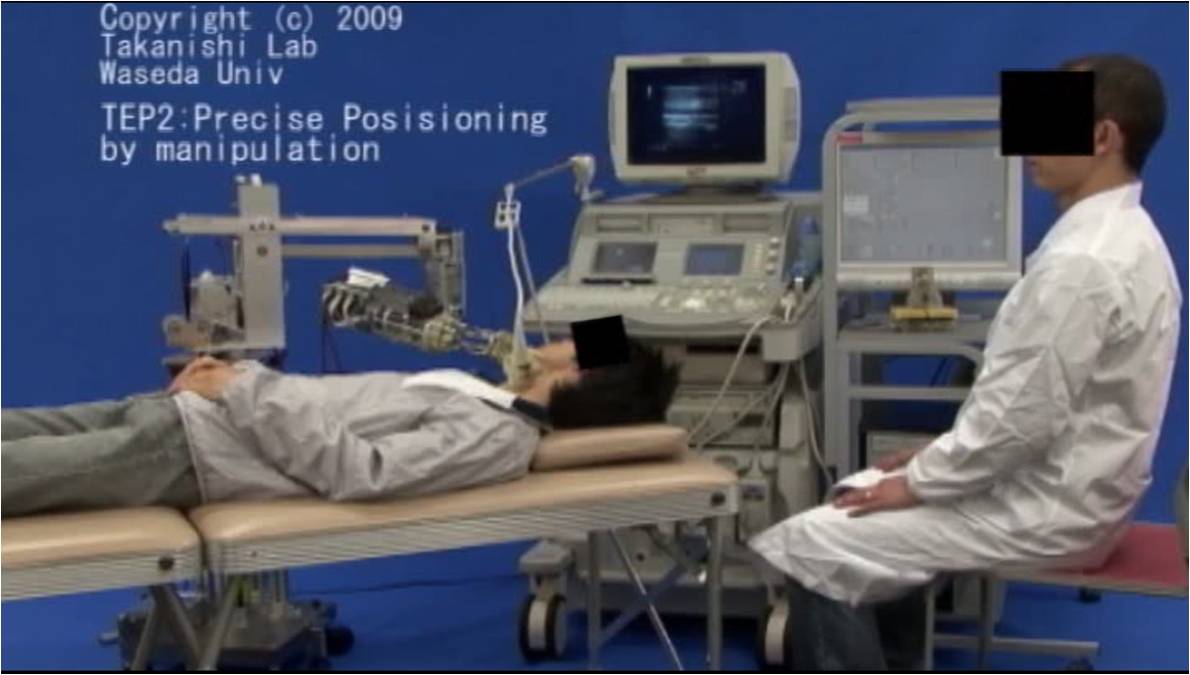
クリックで再生
頸動脈の検出操作 |
ⅰ)操作時間
アームとプローブホルダを用いた大まかな位置決め時間と,マニピュレータを用いた微細な位置決め時間を 本ロボットと旧型機にて比較したところ,操作時間の短縮と操作性の改善が確認された.
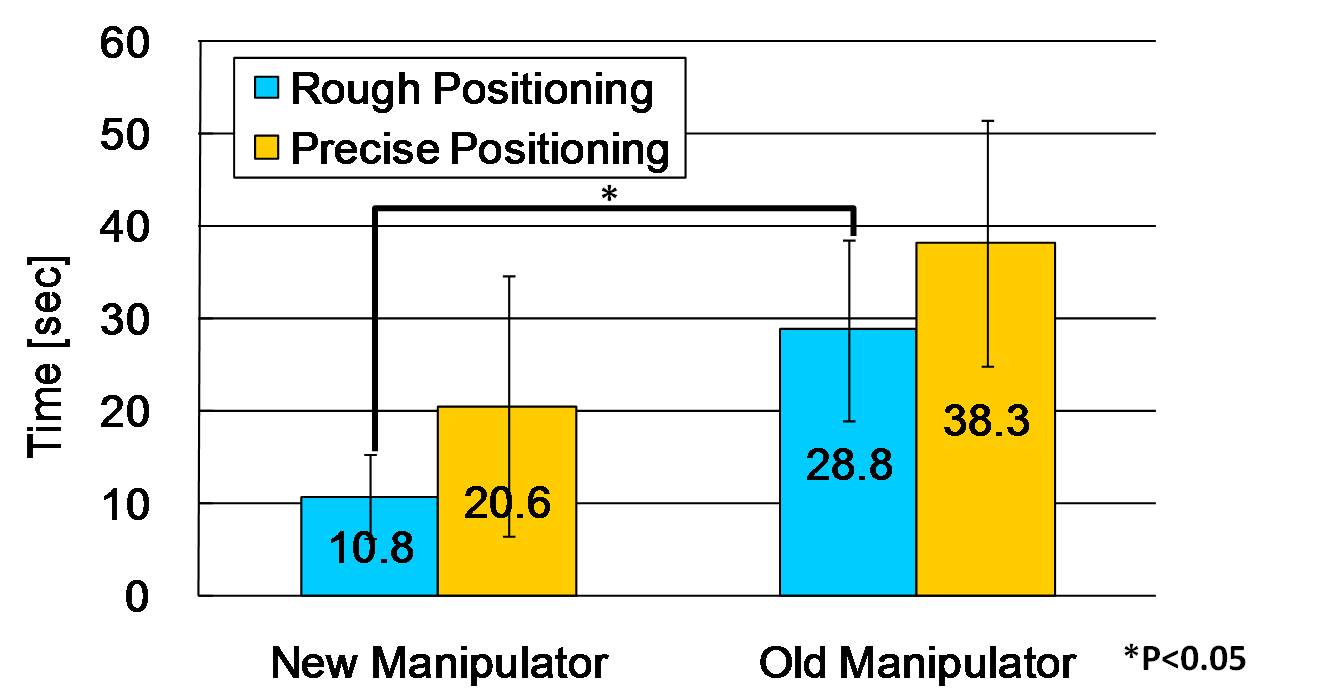
(左:WTA-2R,右:WTA-2)
ⅱ)アンケート
試験を行っていただいた超音波診断技師の方の,本ロボットと旧型機を比較してのアンケートの結果は,
下記のグラフようになった.
アンケート項目は,サイズによる圧迫感,持ちやすさ,大まかな位置決めの行いやすさ,動作の滑らかさとなっており,
全体的に向上したとの評価が得られた.
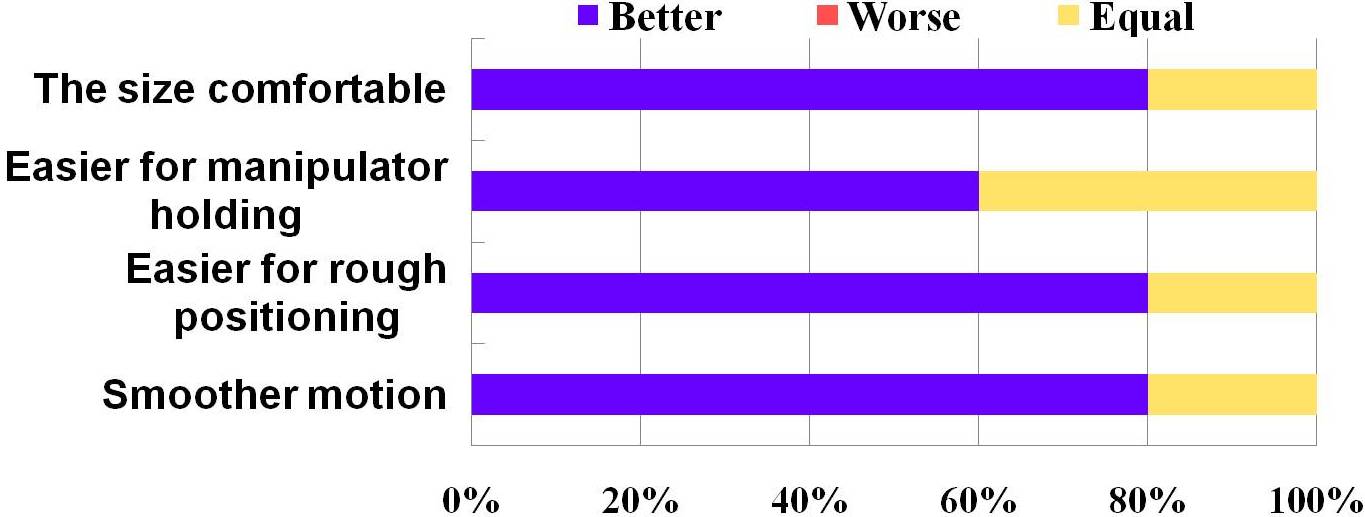
(3)自動位置決めアルゴリズム評価試験
自動位置決めアルゴリズムをロボットに実装し,健常被験者男女11名に対し,
各5回の試験を行い,その成功率を評価した.
試験内容としては,超音波プローブを被験者の頸部右側表皮の上方約5mmの地点に,
マニピュレータがおおよそ被験者の体幹と垂直,かつ,頸部表皮の法線方向と
プローブの向きが一致するようにセットし,自動探索を開始させた.
評価としては,頸動脈を見失って復帰しそうもない場合は試験を中断し,その試験は失敗とし,
頸動脈を発見し角度調整を経て内膜描出まで完了したものを成功とした.
結果は,内膜探索を終え,WI計測準備完了までたどり着いたものは全体の91%となった.
5.謝辞・リンク
共同研究者である姫路獨協大学の菅原基晃先生,東京都市大学の仁木清美先生,
東京女子医科大学の斉藤明子先生,日立アロカメディカル株式会社の皆様に感謝いたします.
また,3DCADソフトウェアをご提供して頂いた ソリッドワークス・ジャパン(株),
マイクロコントローラを提供して頂いたSTマイクロエレクトロニクス(株),球面軸受の特注に対応頂いたヒーハイスト精工(株)に感謝いたします.
本研究は早稲田大学の人を対象とする研究等倫理審査委員会の許可を得て実験を行っています.
|
|
 東京都市大学
東京都市大学
|
|
|
 日立アロカメディカル株式会社
日立アロカメディカル株式会社
|
 ソリッドワークス・ジャパン株式会社
ソリッドワークス・ジャパン株式会社
|
|
|
 ヒーハイスト精工株式会社
ヒーハイスト精工株式会社
|
| 研究紹介ページに戻る | ホームページに戻る |
Copyright(C) 2011 Takanishi Laboratory All Rights Reserved. |